FOGLIO ILLUSTRATIVO
DEALGIC 75 mg capsule rigide a rilascio prolungato
DEALGIC 100 mg capsule rigide a rilascio prolungato
diclofenac sodico
Elenco capitoli
- COMPOSIZIONE
- FORMA FARMACEUTICA E CONFEZIONE
- CATEGORIA FARMACOTERAPEUTICA
- INDICAZIONI
- CONTROINDICAZIONI
- PRECAUZIONI DI IMPIEGO
- INTERAZIONI
- AVVERTENZE
- SOVRADOSAGGIO
- EFFETTI INDESIDERATI
COMPOSIZIONE
una capsula da 100 mg contiene:
pellets gastroresistenti: diclofenac sodico mg 25 pari a diclofenac mg 23,20;
pellets ritardo: diclofenac sodico mg 75 pari a diclofenac mg 69,60; eccipienti: cellulosa microcristallina; polivinilpirrolidone; silice anidra colloidale; copolimero dell’acido metacrilico tipo C; propilenglicole; Eudragit RS 100; Eudragit RL 100; dibutil-ftalato; talco; componenti la capsula di gelatina: acqua depurata; indigotina (E 132); titanio biossido (E 171); gelatina.
una capsula da 75 mg contiene:
pellets gastroresistenti: diclofenac sodico mg 25 pari a diclofenac mg 23,20;
pellets ritardo: diclofenac sodico mg 50 pari a diclofenac mg 46,40; eccipienti: cellulosa microcristallina; polivinilpirrolidone; silice anidra colloidale; copolimero dell’acido metacrilico tipo C; propilenglicole; Eudragit RS 100;
Eudragit RL 100; dibutil-ftalato; talco; componenti la capsula di gelatina: acqua depurata; indigotina (E 132); titanio biossido (E 171); gelatina.
FORMA FARMACEUTICA E CONFEZIONE
20 capsule rigide a rilascio prolungato da 100 mg 20 capsule rigide a rilascio prolungato da 75 mg
E’ possibile che non tutte le confezioni siano commercializzate.
CATEGORIA FARMACOTERAPEUTICA
Antiinfiammatorio non steroideo.
TITOLARE DELL’AUTORIZZAZIONE ALL’IMMISSIONE IN COMMERCIO
Farma Group S.r.l.,
Via Strampelli 18 63074 San Benedetto del Tronto – ASCOLI PICENO (AP)
PRODUTTORE
Temmler Werke GmbH: Weihenstephaner Strasse 28-81673 Monaco. Germania
Doppel Farmaceutici S.r.l.: via Volturno 48-20089 Quinto de’ Stampi-Rozzano
(MI)
INDICAZIONI
Affezioni reumatiche infiammatorie e degenerative: artrite reumatoide, spondilite anchilosante; artrosi: reumatismo extra-articolare; stati dolorosi da flogosi di origine extra-reumatica o post-traumatica.
Trattamento sintomatico della dismenorrea primaria.
CONTROINDICAZIONI
Ipersensibilità verso uno o più componenti del farmaco.
Storia di emorragia gastrointestinale o perforazione relativa a precedenti trattamenti attivi o storia di emorragia/ulcera peptica ricorrente (due o più episodi distinti di dimostrata ulcerazione o sanguinamento).
Grave insufficienza cardiaca.
Cardiopatia conclamata e/o vascolopatia cerebrale (ad es. attacco cardiaco, ictus, mini ictus (TIA) o ostruzione dei vasi sanguigni diretti al cuore o al cervello o un intervento per eliminare o evitare tali ostruzioni.
Il prodotto non deve essere usato:
- in pazienti che soffrono o hanno sofferto di problemi di circolazione sanguigna (arteriopatia periferica). Prima di assumere diclofenac assicurarsi che il proprio medico sia al corrente.
- in pazienti che fumano
- in pazienti che soffrono di diabete
- in pazienti che soffrono di angina, coaguli ematici, pressione del sangue elevata, colesterolo aumentato o trigliceridi aumentati.
Gli effetti indesiderati possono essere ridotti al minimo usando la minima dose efficace per la minima durata necessaria.
Il prodotto non deve essere usato in caso di gravi turbe gastroenteriche, di insufficienza renale e/o epatica grave, in gravidanza, durante l’allattamento, in caso di terapia diuretica intensiva, in soggetti con emorragie in atto e diatesi emorragica, in caso di alterazioni dell’emopoiesi, in corso di trattamento concomitante con anticoagulanti con i quali il diclofenac ha un effetto sinergico.
Come altri antinfiammatori non steroidei, il diclofenac è controindicato in quei soggetti nei quali si sono verificati, dopo assunzione di acido acetilsalicilico o di altri farmaci inibitori della prostaglandin-sintetasi, accessi asmatici, orticaria, riniti acute.
Il prodotto, per il suo dosaggio, è indicato solo nei pazienti adulti.
Non utilizzare in pazienti al di sotto dei 14 anni.
PRECAUZIONI DI IMPIEGO
L’uso di DEALGIC (diclofenac) deve essere evitato in concomitanza di FANS,
inclusi gli inibitori selettivi della COX-2.
Gli effetti indesiderati possono essere minimizzati con l’uso della più bassa dose efficace per la più breve durata di trattamento che occorre per controllare i sintomi.
Anziani: i pazienti anziani hanno un aumento della frequenza di reazioni avverse ai FANS, specialmente emorragie e perforazioni gastrointestinali, che possono essere fatali (vedi “Dose, modo e tempo di somministrazione”).
Emorragia gastrointestinale, ulcerazione e perforazione: durante il trattamento con tutti i FANS, in qualsiasi momento, con o senza sintomi di preavviso o precedente storia di gravi eventi gastrointestinali, sono state riportate emorragia gastrointestinale, ulcerazione e perforazione, che possono essere fatali.
Negli anziani e in pazienti con storia di ulcera, soprattutto se complicata da emorragia o perforazione (vedi “Controindicazioni”), il rischio di emorragia gastrointestinale, ulcerazione o perforazione è più alto con dosi aumentate di
FANS. Questi pazienti devono iniziare il trattamento con la più bassa dose disponibile. L’uso concomitante di agenti protettori (misoprostolo o inibitori di pompa protonica) deve essere considerato per questi pazienti e anche per pazienti che assumono basse dosi di aspirina o altri farmaci che possono aumentare il rischio di eventi gastrointestinali (vedi sotto “Interazioni”).
Pazienti con storia di tossicità gastrointestinale, in particolare anziani, devono riferire qualsiasi sintomo gastrointestinale inusuale (soprattutto emorragia gastrointestinale) in particolare nelle fasi iniziali del trattamento.
Cautela deve essere prestata ai pazienti che assumono farmaci concomitanti che potrebbero aumentare il rischio di ulcerazione o emorragia, come corticosteroidi orali, anticoagulanti come warfarin, inibitori selettivi del reuptake della serotonina o agenti antiaggreganti come l’aspirina (vedi “Interazioni”).
Quando si verifica emorragia o ulcerazione gastrointestinale in pazienti che assumono DEALGIC (diclofenac), il trattamento deve essere sospeso.
I FANS devono essere somministrati con cautela nei pazienti con una storia di malattia gastrointestinale (colite ulcerosa, morbo di Crohn) poiché tali condizioni possono essere esacerbate (vedi “Effetti indesiderati”).
Diagnosi accurata e stretta sorveglianza medica sono obbligatorie in pazienti affetti da grave insufficienza epatica. Nel caso in cui i parametri di funzionalità epatica risultassero persistentemente alterati o peggiorati, il trattamento con
DEALGIC deve essere interrotto.
Particolare cautela deve essere posta nei pazienti con porfiria epatica, in quanto il diclofenac potrebbe scatenare un attacco.
Per l’interazione col metabolismo dell’acido arachidonico, il farmaco può determinare in asmatici e soggetti predisposti crisi di broncospasmo ed eventualmente shock ed altri fenomeni allergici.
Occorre cautela nei pazienti con una storia di ipertensione e/o insufficienza cardiaca poiché, in associazione alla terapia con FANS, sono state riportate ritenzione idrica ed edema.
Gravi reazioni cutanee alcune delle quali fatali, includenti dermatite esfoliativa, sindrome di Stevens-Johnson e necrolisi tossica epidermica, sono state riportate molto raramente in associazione con l’uso dei FANS (vedi “Effetti indesiderati”).
Nelle prime fasi della terapia i pazienti sembrano essere a più alto rischio: l’insorgenza della reazione si verifica nella maggior parte dei casi entro il primo mese di trattamento. DEALGIC (diclofenac) deve essere interrotto alla prima comparsa di rash cutaneo, lesioni della mucosa o qualsiasi altro segno di ipersensibilità.
A causa dell’importanza delle prostaglandine per il mantenimento del flusso ematico renale, è richiesta particolare cautela o si impone l’esclusione dall’uso di
DEALGIC in caso di ipoperfusione renale, insufficienza cardiaca o renale, ipertensione arteriosa, fenomeni tromboembolici all’anamnesi, in pazienti in trattamento con diuretici e in quelli reduci da interventi chirurgici maggiori, nonché in pazienti in età avanzata.
Durante trattamenti prolungati con DEALGIC come con altri antinfiammatori non steroidei altamente attivi, sono indicati come misura precauzionale controlli della crasi ematica e della funzionalità epatica e renale.
Nel trattamento dei pazienti anziani o sotto peso si raccomanda di somministrare il più basso dosaggio efficace.
INTERAZIONI
Corticosteroidi: aumento del rischio di ulcerazione o emorragia gastrointestinale (vedi “Precauzioni per l’uso”).
Anticoagulanti: i FANS possono aumentare gli effetti degli anticoagulanti, come il warfarin (vedi “Precauzioni per l’uso”).
Agenti antiaggreganti e inibitori selettivi del reuptake della serotonina (SSRIs): aumento del rischio di emorragia gastrointestinale (vedi “Precauzioni per l’uso”).
Diuretici, ACE inibitori e antagonisti dell’angiotensina II
I FANS possono ridurre l’effetto dei diuretici e di altri farmaci antiipertensivi.
In alcuni pazienti con funzione renale compromessa (per esempio pazienti disidratati o pazienti anziani con funzione renale compromessa), la co-somministrazione di un ACE
inibitore o di un antagonista dell’angiotensina II e di agenti che inibiscono il sistema della ciclo-ossigenasi può portare a un ulteriore deterioramento della funzione renale, che comprende una possibile insufficienza renale acuta, generalmente reversibile.
Queste interazioni devono essere considerate in pazienti che assumono DEALGIC
in concomitanza con ACE inibitori o antagonisti dell’angiotensina II.
Quindi, la combinazione deve essere somministrata con cautela, specialmente nei pazienti anziani.
I pazienti devono essere adeguatamente idratati e deve essere preso in considerazione il monitoraggio della funzione renale dopo l’inizio della terapia concomitante.
Se somministrato insieme ad altre preparazioni contenenti digossina, il diclofenac ne può elevare la concentrazione plasmatica, ma in tali casi non sono stati ancora osservati segni clinici di sovradosaggio. Sconsigliabile la contemporanea somministrazione di sali di Litio in quanto può dar luogo ad aumento della litiemia.
Diversi antiinfiammatori non steroidei possono inibire l’attività dei diuretici e potenziare l’effetto dei diuretici K-risparmiatori, rendendo necessario il controllo dei livelli sierici del potassio.
Sebbene gli studi clinici non sembrino indicare che DEALGIC abbia effetti sugli anticoagulanti, sono stati osservati casi isolati di aumento del rischio di emorragia con l’uso combinato di diclofenac sodico e una terapia anticoagulante.
Si raccomanda una stretta sorveglianza di tali pazienti. Come altri FANS il diclofenac ad alte dosi può temporaneamente inibire l’aggregazione piastrinica.
La somministrazione di antiinfìammatori non steroidei meno di 24 ore prima o dopo il trattamento con metotrexate va fatta con cautela, poiché tali farmaci possono elevarne la concentrazione ematica ed aumentarne la tossicità.
Anche se largamente legato alle proteine, il diclofenac non interferisce per esempio col legame proteico di: salicilati, tolbutamide, prednisolone.
Il prodotto non aumenta l’effetto ipoglicemizzante di: tolbutamide, biguanidi, glibenclamide e non influenza negativamente il metabolismo del glucosio in diabetici e soggetti sani.
DEALGIC può aumentare la nefrotossicità della ciclosporina attraverso il suo effetto inibitorio sulle prostaglandine del rene.
AVVERTENZE
Le medicine come DEALGIC possono essere associate ad un modesto aumento del rischio di attacco cardiaco (“infarto del miocardio”) o ictus. Qualsiasi rischio è più probabile con alte dosi e trattamenti prolungati. Non superare la dose o la durata del trattamento raccomandata.
Se ha problemi cardiaci, o precedenti di ictus o pensa di potere essere a rischio per queste condizioni (per esempio se ha la pressione sanguigna alta, diabete o colesterolo elevato o è un fumatore) deve discutere la sua terapia con il suo dottore o farmacista.
Il prodotto non deve essere usato durante la gravidanza o l’allattamento.
I pazienti che manifestano capogiri o altri disturbi nervosi centrali dovrebbero astenersi dal guidare un veicolo o dall’utilizzare macchinari che richiedono integrità del grado di vigilanza, specie sotto l’effetto contemporaneo dell’alcool.
L’uso di DEALGIC, come di qualsiasi farmaco inibitore della sintesi delle prostaglandine e della cicloossigenasi è sconsigliato nelle donne che intendano iniziare una gravidanza.
L’inibizione della sintesi di prostaglandine può interessare negativamente la gravidanza e/o lo sviluppo embrio/fetale.
Risultati di studi epidemiologici suggeriscono un aumentato rischio di aborto e di malformazione cardiaca e di gastroschisi dopo l’uso di un inibitore della sintesi delle prostaglandine nelle prime fasi della gravidanza. Il rischio assoluto di malformazioni cardiache aumentava da meno dell’1%, fino a circa l’1,5 %. E’
stato ritenuto che il rischio aumenta con la dose e la durata della terapia.
Negli animali, la somministrazione di inibitori della sintesi di prostaglandine ha mostrato di provocare un aumento della perdita di pre e post-impianto e di mortalità embrione-fetale.
Inoltre, un aumento di incidenza di varie malformazioni, inclusa quella cardiovascolare, è stato riportato in animali a cui erano stati somministrati inibitori di sintesi delle prostaglandine, durante il periodo organogenetico.
Durante il terzo trimestre di gravidanza, tutti gli inibitori della sintesi di prostaglandine possono esporre il feto a: la madre e il neonato, alla fine della gravidanza, a:
- tossicità cardiopolmonare (con chiusura prematura del dotto arterioso e ipertensione polmonare);
- disfunzione renale, che può progredire in insufficienza renale con oligo-idroamnios;
- possibile prolungamento del tempo di sanguinamento ed effetto antiaggregante che può occorrere anche a dosi molto basse;
- inibizione delle contrazioni uterine risultanti in ritardo o prolungamento del travaglio.
La somministrazione di DEALGIC dovrebbe essere sospesa nelle donne che hanno problemi di fertilità o che sono sottoposte a indagini sulla fertilità.
DOSE, MODO E TEMPO DI SOMMINISTRAZIONE
A seconda della gravità della malattia:
Adulti: 1 capsula di DEALGIC 100 mg capsule rigide a rilascio prolungato o di
DEALGIC 75 mg capsule rigide a rilascio prolungato 1 volta al dì.
Se necessario, la dose giornaliera può essere aumentata fino a 150 mg, somministrando 1 capsula di DEALGIC 75 mg capsule rigide a rilascio prolungato 2 volte al dì, oppure 2 capsule in un’unica somministrazione, in presenza di disturbi particolarmente gravi, specie mattutini.
Il farmaco va ingerito senza masticare e con sufficiente quantità di liquido.
L’assunzione dopo i pasti può ritardare il passaggio in circolo del principio attivo.
Pertanto DEALGIC, in caso di dolori acuti, dovrebbe essere assunto prima dei pasti.
La durata del trattamento varia a seconda del caso.
SOVRADOSAGGIO
II trattamento dell’avvelenamento acuto da antiinfiammatori non steroidei consiste essenzialmente in misure di supporto e sintomatiche. Nulla si sa ancora riguardo al quadro clinico risultante da un sovradosaggio di diclofenac.
Le misure terapeutiche da adottare in caso di sovradosaggio sono le seguenti:
- l’assorbimento deve essere impedito non appena possibile per mezzo di lavanda gastrica e trattamento con carbone attivo;
- trattamenti di sostegno e sintomatici dovrebbero essere adottati in caso di complicazioni (ipotensione, insufficienza renale, convulsioni, irritazione gastrointestinale e depressione respiratoria);
- terapie specifiche come diuresi forzata, dialisi o emoperfusione, non sono probabilmente di alcuna utilità nell’eliminare gli antiinfiammatori non steroidei, a causa del loro elevato legame con le proteine plasmatiche e del loro notevole metabolismo.
EFFETTI INDESIDERATI
Gastrointestinali: gli eventi avversi più comunemente osservati sono di natura gastrointestinale.
Possono verificarsi ulcere peptiche, perforazione o emorragia gastrointestinale, a volte fatale, in particolare negli anziani (vedi “Precauzioni per l’uso”).
Dopo somministrazione di DEALGIC (diclofenac) sono stati riportati: nausea, vomito, diarrea, flatulenza, costipazione, dispepsia, dolore addominale, melena, ematemesi, stomatiti ulcerative, esacerbazione di colite e morbo di Crohn (vedi “Precauzioni per l’uso”).
Meno frequentemente sono state osservate gastriti.
Edema, ipertensione e insufficienza cardiaca sono state riportate in associazione al trattamento con FANS.
Le medicine come DEALGIC possono essere associate ad un modesto aumento del rischio di attacco cardiaco (“infarto del miocardio”) o ictus.
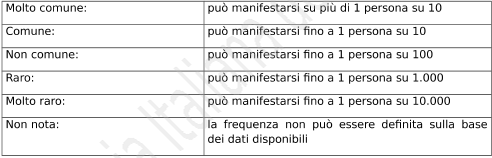
Raramente possono comparire manifestazioni allergiche come rash cutaneo, prurito, edema, accessi asmatici e/o reazioni anafilattiche o anafilattoidi, accompagnati o meno da ipotensione.
Di eccezionale evenienza sono le reazioni di fotosensibilità e reazioni cutanee gravi quali eritema essudativo multiforme e reazioni bollose includenti sindrome di Stevens Johnson e necrolisi tossica epidermica (molto raramente).
Sporadicamente sono state segnalate turbe del SNC come cefalea, eccitazione, irritabilità, insonnia, astenia, capogiri, convulsioni, disturbi sensori o della visione, acufeni.
Particolarmente in trattamenti protratti possono verificarsi edemi periferici, insufficienza renale, sindrome nefrotica, aumento delle transaminasi, ittero, alterazioni dell’emopoiesi (leucopenia, trombocitopenia, agranulocitosi, anemia aplastica o emolitica), perdita di capelli.
In casi isolati: anomalie urinarie, nefrite interstiziale, disturbi della funzionalità epatica, compresa epatite con o senza ittero, in alcuni rari casi fulminante.
Segnalare al medico curante qualsiasi reazione indesiderata non prevista dal foglio illustrativo.
Attenzione: non utilizzare il medicinale dopo la data di scadenza indicata sulla confezione.
Tenere il medicinale fuori dalla portata e dalla vista dei bambini.
Conservare le capsule al riparo dalla luce e dall’umidità.
REVISIONE DEL FOGLIO ILLUSTRATIVO DA PARTE DELL’AGENZIA ITALIANA DEL FARMACO: Ottobre 2012